Tin tức, Kiến thức hóa chất, Kiến thức Soda
Phương trình nhiệt phân NaHCO3 và những điều cần biết
Nhiệt phân NaHCO3 là một phản ứng hóa học quan trọng, thường được nhắc đến trong nhiều ngành công nghiệp và ứng dụng đời sống hàng ngày. Phản ứng này không chỉ giúp tạo ra các hợp chất quan trọng mà còn mang ý nghĩa trong việc xử lý môi trường và thực phẩm. Trong bài viết này, chúng ta sẽ tìm hiểu chi tiết về phản ứng nhiệt phân NaHCO3, từ khái niệm cơ bản, phương trình, đến các ứng dụng thực tế nổi bật.
1. NaHCO3 là gì?
NaHCO3 (natri bicarbonate) hay còn gọi là “baking soda” là một hợp chất hóa học quen thuộc. Đây là muối của axit cacbonic, mang tính lưỡng tính, nghĩa là có khả năng phản ứng với cả axit và bazơ.

1.1. Tính chất vật lý
- Công thức hóa học: NaHCO3.
- Trạng thái: Tinh thể màu trắng hoặc dạng bột mịn, không mùi.
- Khối lượng mol: 84,01 g/mol.
- Độ tan trong nước: 96 g/L ở 20°C, tạo dung dịch có tính kiềm nhẹ.
- Điểm nóng chảy: Không nóng chảy mà phân hủy ở nhiệt độ khoảng 50°C – 60°C.
- Hương vị: Có vị hơi mặn, giống muối.
1.2. Tính chất hóa học
Tính chất lưỡng tính: NaHCO3 có thể phản ứng với cả axit và bazơ:
- Với axit mạnh, giải phóng CO2: NaHCO3+HCl→NaCl+H2O+CO2
- Với bazơ mạnh, tạo ra muối và nước: NaHCO3+NaOH→Na2CO3+H2O
Phản ứng nhiệt phân: Khi đun nóng, NaHCO3 phân hủy thành natri cacbonat (Na2CO3), khí CO2 và hơi nước:
2NaHCO3 (nhiệt độ)→ Na2CO3 + CO2 + H2O
2. Hướng dẫn thí nghiệm phản ứng nhiệt phân NaHCO3 ra Na2CO3
2.1. Giai đoạn chuẩn bị
Trước khi bắt đầu thí nghiệm, chúng ta cần chuẩn bị các dụng cụ sau:
- 1 ống nghiệm
- 1 nút cao su
- 1 cốc chứa dung dịch nước vôi trong Ca (OH)2
- 1 đèn cồn
- 1 giá đỡ thí nghiệm
- 1 ống dẫn khí
- Hóa chất NaHCO3, dung dịch nước vôi trong Ca (OH)2
- Dụng cụ bảo hộ khi thực hiện thí nghiệm
2.2. Các bước thí nghiệm nhiệt phân NaHCO3 ra Na2CO3
Bước 1: Chuẩn bị: Lấy một muỗng bột Natri Hidrocacbonat (NaHCO3) cho vào ống nghiệm. Sau đó, đậy kín ống nghiệm bằng nút cao su có ống dẫn khí và đặt ống lên giá thí nghiệm.
Bước 2: Kết nối: Đầu ra của ống dẫn khí được nhúng vào một cốc chứa dung dịch nước vôi trong (Ca(OH)₂).
Bước 3: Hơ nóng: Tiến hành hơ nóng đều toàn bộ ống nghiệm để chuẩn bị cho phản ứng.
Bước 4: Đun tập trung: Đun nóng tập trung tại vị trí chứa bột NaHCO3 trong ống nghiệm. Quan sát kỹ hiện tượng xảy ra trong ống nghiệm và cốc chứa nước vôi trong.
Bước 5: Kết quả: Ghi nhận các hiện tượng để phân tích kết quả thí nghiệm nhiệt phân NaHCO3.
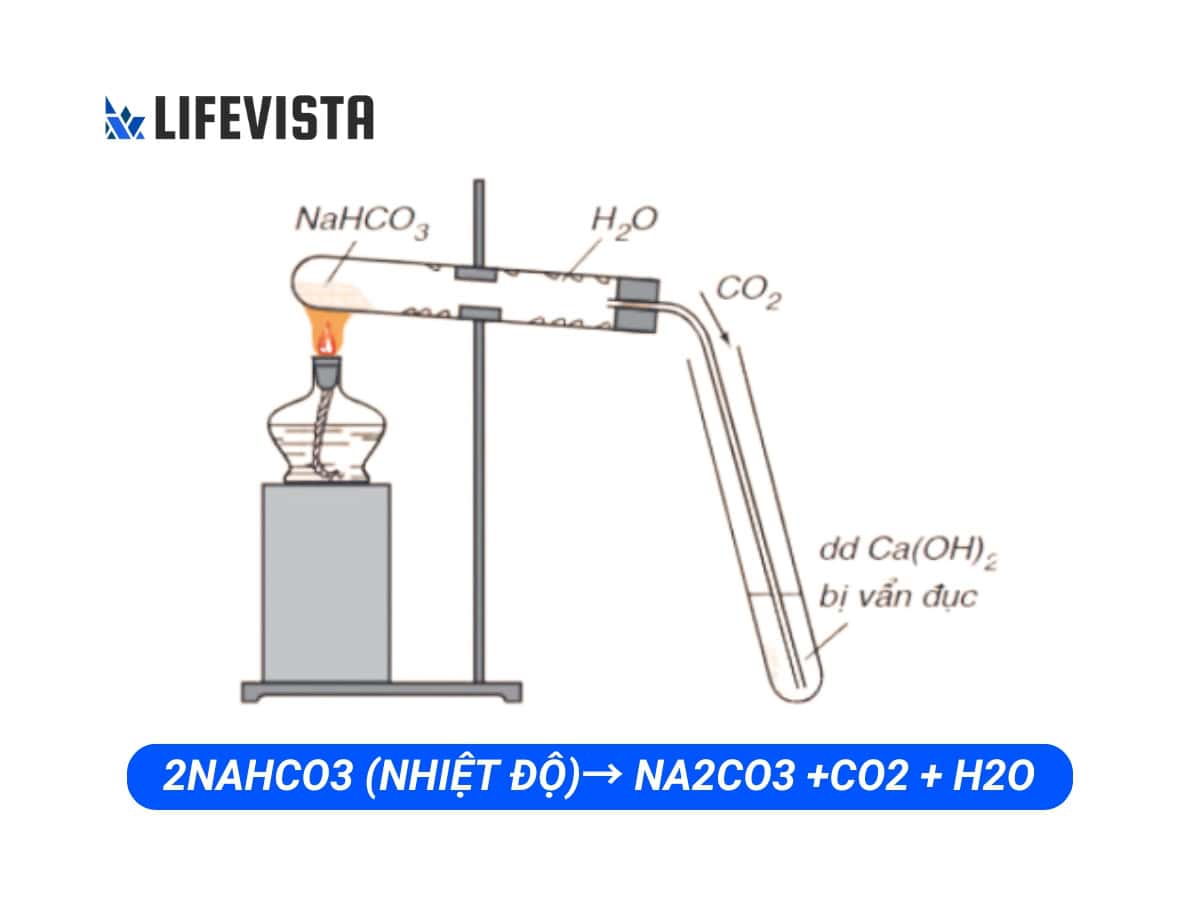
2.3. Kết quả sau thí nghiệm nhiệt phân NaHCO3 ra Na2CO3
Trong ống nghiệm chứa NaHCO3:
- Trên thành ống nghiệm: Xuất hiện các giọt nước li ti đọng lại, chứng tỏ phản ứng nhiệt phân đã tạo ra nước.
- Khí thoát ra: Khí CO2 sinh ra từ quá trình nhiệt phân đi qua ống dẫn khí ra ngoài.
- Kết tủa tại đáy ống nghiệm: Hình thành chất rắn màu trắng là muối mới Natri Cacbonat (Na2CO3), hay còn gọi là Soda. Vì Na2CO3 có nhiệt độ nóng chảy cao (851°C), dưới ngọn đèn cồn, chất này không nóng chảy mà tồn tại dưới dạng kết tủa rắn.
Trong cốc dung dịch nước vôi trong Ca(OH)2:
- Phản ứng với khí CO2: Khí CO2 thoát ra phản ứng với Ca(OH)2 trong dung dịch, tạo ra hiện tượng vẩn đục do sự hình thành của kết tủa Canxi Cacbonat (CaCO3).
- Phản ứng tiếp theo: Nếu tiếp tục đun nóng NaHCO33 lượng CO2 sinh ra nhiều sẽ hòa tan kết tủa vẩn đục này, làm dung dịch trong trở lại.
Nhìn chung, nhiệt phân NaHCO3 là phương pháp phổ biến và đơn giản để điều chế Na2CO3 (Soda). Dấu hiệu đặc trưng của phản ứng là sự giải phóng khí CO2, tạo thành kết tủa trắng trong ống nghiệm và vẩn đục trong dung dịch nước vôi trong.
2.4. Phương trình phản ứng nhiệt phân NaHCO3 ra Na2CO3
Phương trình nhiệt phân NaHCO3 dưới nhiệt độ cao. NaHCO3 sẽ bị phân hủy tạo thành muối Natri cacbonat (Sodium carbonate), giải phóng khí cacbonic:
|
2NaHCO3 |
(nhiệt độ)→ | Na2CO3 | + | CO2↑ | + | H2O |
|
Natri Hidrocacbonat |
Natri Cacbonat | Cacbonic | Nước | |||
| (Rắn) | (Rắn) | (Khí) |
(Khí) |
|||
| Màu trắng | Màu trắng | Không màu |
Không màu |
3. Những ứng dụng thực tế của phản ứng nhiệt phân NaHCO3
Phản ứng nhiệt phân NaHCO3 tạo ra ba sản phẩm gồm nước, khí CO2 và muối Na2CO3. Bên cạnh ứng dụng quen thuộc của nước, khí CO2 và muối Na2CO3 cũng được sử dụng rộng rãi trong nhiều lĩnh vực của cuộc sống.
3.1. Tạo ra muối Na2CO3 hay Soda Na2CO3
Đun nóng NaHCO3 là một trong những phương pháp đơn giản và hiệu quả để điều chế Soda (Na2CO3). Trong công nghiệp, quy trình sản xuất Soda được thực hiện theo phương pháp Solvay, sử dụng amoniac. Quá trình này bao gồm bước đầu điều chế NaHCO3, sau đó đun nóng để thu được Na2CO3.
Soda tồn tại ở dạng bột rắn màu trắng và có nhiều ứng dụng quan trọng trong y học, công nghiệp sản xuất, công nghiệp thực phẩm. Đặc biệt, sau khi được điều chế, Soda còn được sử dụng phổ biến trong xử lý nước bể bơi, với liều lượng khuyến nghị từ 1 – 3 kg/100 m3 nước.
Na2CO3 là hóa chất cân bằng nồng độ pH trong nước bể bơi một cách nhanh chóng. Là một bazơ mạnh, Na2CO3 còn phản ứng với các kim loại có tính chất yếu như magie và canxi, giúp loại bỏ tạp chất và làm sạch nước hồ bơi hiệu quả.

3.2. Ứng dụng làm sạch các chất bị ô nhiễm axit
Phản ứng nhiệt phân NaHCO3 tạo ra Na2CO3 được ứng dụng phổ biến trong việc xử lý các chất ô nhiễm axit và tái chế dư lượng từ các phản ứng liên quan. Quá trình này bao gồm các phản ứng hóa học chính như sau:
- NaHCO3 nhiệt phân tạo ra muối Na2CO3: 2NaHCO3 → Na2CO3 +CO2↑ + H2O
- Muối Na2CO3 tiếp tục phản ứng với các chất ô nhiễm axit để tạo thành natri clorua và natri sunfit:
NaHCO3 + HCl → NaCl + CO2+ H2O
2NaHCO3 + SO2 → Na2SO3 + 2CO2 + H2O
- Sau đó, khi có khí O2, Na2SO3 có thể chuyển thành NaSO4 – muối trung hòa: 2Na2SO3 + O2 → 2Na2SO4
3.3. Giải phóng khí CO2 – Chất dập lửa
Phản ứng nhiệt phân NaHCO3 được ứng dụng hiệu quả để dập tắt các đám cháy nhỏ do dầu mỡ hoặc cháy điện. Khi bột NaHCO3 được ném vào ngọn lửa, nhiệt độ cao sẽ khiến nó phân hủy và giải phóng khí CO2. Do CO2 nặng hơn và không phản ứng với O2, nó tạo thành một lớp bao phủ, ngăn cản oxy tiếp xúc với ngọn lửa, từ đó dập cháy nhanh chóng. Đây cũng là lý do khí CO2 được sử dụng rộng rãi trong các thiết bị chữa cháy.
Tuy nhiên, đối với các đám cháy dầu mỡ lớn hoặc trong nồi chiên nhúng, không nên dùng phương pháp này. Khí CO2 thoát ra đột ngột có thể khiến dầu mỡ và ngọn lửa bắn tung tóe, làm tình hình trở nên nguy hiểm hơn.
Ngoài ra, nhờ khả năng tạo ra khí CO2, NaHCO3 còn được sử dụng trong bình chữa cháy hóa chất khô loại BC. So với photphat diammonium, một chất ăn mòn cao hơn thường dùng trong bình chữa cháy loại ABC, NaHCO3 là một lựa chọn thay thế an toàn và ít ăn mòn hơn.
3.4. Tăng độ xốp cho các loại bánh
Phản ứng nhiệt phân NaHCO3 ra Na2CO3 được ứng dụng phổ biến trong làm bánh và sản xuất bột nở. Chất này giúp tạo độ xốp cho nhiều loại bánh như bánh quẩy, bánh bông lan, bánh biscuits…
Không chỉ giúp bánh xốp, NaHCO3 còn hoạt động như một chất tạo men, phản ứng với axit có trong nguyên liệu để giải phóng khí CO2. Khí này làm cho bánh nở đều, mang lại kết cấu mềm mại và hương vị thơm ngon hơn.
Ngay cả khi nguyên liệu không chứa axit, phản ứng nhiệt phân của NaHCO3 vẫn tạo ra Na2CO3 có tính kiềm mạnh. Tính chất này không chỉ giúp bánh có màu vàng bắt mắt mà còn mang lại vị hơi đặc trưng, hấp dẫn hơn cho thành phẩm.

3.5. Sử dụng trong chế biến thức ăn
Baking soda có thể được sử dụng trực tiếp trong nấu ăn với liều lượng khuyến nghị để cải thiện chất lượng món ăn. Nó giúp thức ăn nhanh mềm hơn, đặc biệt hiệu quả với các món hầm, ninh, hoặc kho. Đối với rau luộc, baking soda giữ cho màu xanh tươi của rau, ngăn chặn sự chuyển màu vàng trong quá trình nấu. Ngoài ra, baking soda còn làm tăng độ giòn, xốp cho các món chiên, rán, mang lại kết cấu hấp dẫn và hương vị hoàn hảo.
>> Xem thêm: Soda Na2CO3 là gì? Ứng dụng của Na2CO3 trong xử lý nước cứng
4. LifeVista – Đơn vị cung cấp hóa chất Soda Ash Light Na2CO3 chất lượng
LifeVista tự hào là nhà cung cấp các sản phẩm hóa chất chất lượng cao, đặc biệt là các loại Soda Ash Light Na2CO3. Với nguồn hàng phong phú và uy tín trên thị trường, LifeVista cam kết mang đến sản phẩm đạt tiêu chuẩn quốc tế, đáp ứng nhu cầu sử dụng của khách hàng trong công nghiệp và đời sống.
- Chất lượng cao: Hóa chất đạt chuẩn, đảm bảo hiệu quả sử dụng.
- Hỗ trợ tận tình: Đội ngũ tư vấn chuyên nghiệp, cung cấp giải pháp tối ưu cho từng khách hàng.
- Giao hàng nhanh chóng: Đáp ứng đơn hàng trên toàn quốc với thời gian ngắn nhất.
5. Kết
Phản ứng nhiệt phân NaHCO3 không chỉ quan trọng trong hóa học mà còn mang lại nhiều giá trị thiết thực trong đời sống và công nghiệp. Từ sản xuất Na2CO3, xử lý môi trường, đến chế biến thực phẩm, phản ứng này có tính ứng dụng rộng rãi. Nếu bạn cần tìm mua NaHCO3 hoặc hóa chất hồ bơi Soda Ash Light Na2CO3, LifeVista chính là đối tác đáng tin cậy mà bạn có thể lựa chọn.
>> Xem thêm: Xút ăn da là gì? Ứng dụng của xút trong xử lý nước



